
 关注数学发展弘扬科学精神
关注数学发展弘扬科学精神
古希腊名医希波克拉底有一句教导学生的名言:“无损害是最重要的。”可是现代的医生们经常发现,医学中为了诊断疾病,他们必须采用活组织切片和血管造影术这样的极具破坏性的手段。甚至x射线也不是没有损害的。为了治疗疾病,医生们需要看清病人体内的变化。虽然听诊器很有用,可它无法听到癌细胞的生长。
医学研究人员还在不断地寻找更安全和更精确的监视病人的方法。在位于纽约特洛伊的Rensselaer技术学院(Rensselaer Polytechinic Institute,简称RPI)中,一群由数学家和工程师组成的研究小组,就在从事这项研究。数学家大卫·艾萨克和马格丽特·切尼,生物医学工程师乔纳森·纽厄尔和他们的同事一道,发展了一种新的、基于数学的技术。这项技术可以对心脏、肺和其他的器官进行实时的连续成像,既不必动手术切开一个口子,也不用再经受射线的辐射。他们希望他们的仪器(已在奥尔巴尼医学中心投入临床使用),能够最终为医生提供一种更为高效和安全的心脏疾病、肺水肿和乳腺癌等的诊断方法。这一新技术称为电阻抗成像。它的工作原理是:给放置在皮肤上的电极通上很小的电流,测量对应的电压响应,然后推导出体内的电导率和电容率(粗略地说,电导率表示电荷通过介质的难易程度,而电容率表示介质存贮电能的能力)。既然身体的不同部分具有不同的电性质,计算得到的分布就可以提供身体组织和体液的图像。
以肺为例,空气是非常差的导电体。所以,当健康的肺中充满空气时,他们在阻抗成像中显示低电导率的区域。与之形成鲜明对比的是,肺水肿(一种常见于外伤、心脏病或大手术后的并发症)病人的一部分肺中充满了液体;因为液体具有高电导率,肺水肿就可以在阻抗成像中显示为异常。
在左边的容器中,可以看到一根导管和一根绝缘管。这些物体被放置在盐水中,使得盐水刚好浸没电极。RPI研究小组在这些容器中实验他们的阻抗成像。
阻抗成像是几种依赖于数学理论的医学成像技术之一。最常见的是计算机X射线轴向分层造影或CAT扫描。本质上说,CAT扫描把来自不同方向的X射线结合起来。每条X射线标识了身体组织沿着某个方向的密度。一种基于拉东变换的数学技巧的计算机算法,正是利用这些数据,重建出空间中的密度分布。类似地,磁共振成像(MRI)通过测量身体在强磁场下的反应来生成图像。
这些技巧都与求解所谓的反问题有关,因为它们都要求对直接计算求逆。比如,如果物体中的电导分布已知,施加个给定的电流,就可以直接算出电压响应;类似于一个代数表达式2x^2+7x-5,如果变量x的值已知,那么就可以直接代入算出表达式的值。另一方面,反问题(比如从一组测得的电压响应值来重构电导分布)就好比求未知数工,使得2x^2+7x-5等于2,虽然实际问题可能要困难得多。
对阻抗成像来说,需要求解的方程是麦克斯韦方程,一组描述所有电磁现象的偏微分方程。从体表的测量来构建身体内部的图像是相当有挑战性的问题,不但因为方程是非线性的,而且由于重建对于测量误差具有高度的敏感性。艾萨克指出,“差别很大的电导分布有可能得出非常相近的数据”。为了处理这个问题,RPI研究小组设计了高精度的电路系统来输出电流和测量电压,并结合应用计算机算法来优化系统的性能。
RPI小组把他们的仪器命名为第三代自适应电流断层摄影仪(ACT III),它将精密的工程技术、复杂的数学分析和高速的计算机算法结合起来,生成精确的电流模式,并根据测量到的响应值重建出图像。施加到电极的电流与测量心电图时类似,远低于人类所能感知的水平,所以是无害的。这就使得这个系统适合于作为监视设备而能连续使用。CAT扫描只能对身体拍摄快照,而阻抗成像可以生成连续影像,从而跟踪生理过程,而不仅仅是揭示解剖结构。
这并不是说阻抗成像会让CAT扫描变得过时,相反,由于它们检测身体组织的不同性质,这两种技术会是很好的互补。可是阻抗成像有一些特别的优势。首先,它相对便宜,部分原因是它的电子设备更加紧凑。其次,它也并不是非得由专家来操作和解释,ACT III及其更新可以由救护人员在救护车上操作。
艾萨克在20世纪80年代早期就开始研究阻抗成像中的数学问题。他很快就发现只有理论本身是不够的。“我对要做的事有了一些想法,可是我需要对目前测量仪器的精确度有更好的现实了解,所以我需要做一些实验。”他回忆说。于是他找到纽厄尔,虽然后者当时对阻抗成像的实用性表示怀疑,但还是帮助设计了一个实验。他们决定观察艾萨克的电数学理论是否可以定位一盆盐水中的大块凝胶。
“我们从附近的超市买了一个小盘子,装上凝胶和盐水,在盘子外面布上电极,输入电流然后测量电压。”艾萨克回忆说。果真,出现了一幅图像,虽然很粗糙,但还是大致给出了凝胶的位置。艾萨克说,“这一现象让纽厄尔感到非常兴奋。”
纽厄尔找来RPI的退休教授、电子工程师大卫·吉辛,来帮忙设计电子设备。“第一个系统是很粗糙的,但确实管用。”艾萨克说。电流模式在硬件和软件上都做了许多特别的改进。切尼指出,在RPI的位电子工程师加里·索尼埃和他的学生彼得·埃迪克的帮助下,这个系统的速度已经相当快,足够实时使用。“有许多学生在不同时期为这个研究项目做了工作。”切尼补充说。“从我加入这个项目开始,总有10~20个学生参与工作,人数多少与基金资助有关。从博士生到本科生都有。甚至还曾有过那么一两个出色的高中生。”
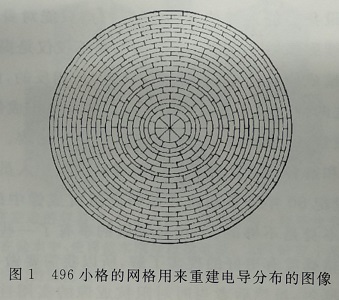
在一个直径30 cm的盘子(大小和形状与人的胸腔相似)周围布满电极,ACT III可以重建出盘子中心一个硬币大小物体的合理图像,这是最难得到图像的点。RPI小组目前正在对人体进行临床实验,包括奥尔巴尼医学中心的志愿者。为了对通过心脏和肺的一个截面成像,研究人员把附有32个电极的带子绑在病人的胸部。接着ACT II向电极输入一组特殊设计的电流模式。在32个电极上测得的电压值反馈到仪器上,然后用一种被RPI小组称为NOSER(牛顿单步误差重建)的算法进行计算来生成一个圆形的496小格的图像(见图2~图4)。输出图像被显示到一个视频监视器上,病人可以清楚地看到自己肺部的收缩和血液的循环:低电导率的空气显示深蓝色,高电导率的血液显示大红色。
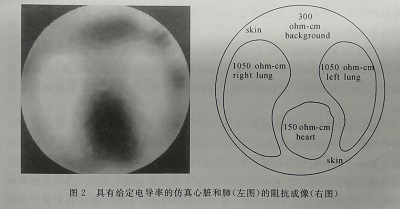

数学上来说,每个电流模式一即从一个电极输入,然后从另一个电极输出,是一个32维空间中的向量数字。更准确地说,每个模式是一个31维子空间中的向量,因为我们要求输入的净电流为零(否则头发就会竖起来了)。测得的电压响应也是一个31维空间中的向量。粗略地说,电导率分布可以在联系电流和电压的矩阵中找到。为了找到这个矩阵,我们必须输入31种基本不同的电流模式(用数学术语说,就是必须线性无关)。
对RPI小组来说,一个关键的问题就是怎样设计合理的电流模式来得到最佳的信号。原则上说,任意31个线性无关的模式都是可行的。可是这忽略了误差的效应,可能使得线性代数的解完全无效。

“我们意识到最好的模式集合依赖于人体的内部。”艾萨克解释道。对于离体表较近区域的成像,采用一个电极送电,在附近一个电极处测量的模式是最优的。RPI小组还采用基于三角的正弦和余弦函数的模式。这些模式可以证明对于检测较深入的人体内部是最有效的。艾萨克和他的同事发展了一套数学理论,使得ACT III可以自己计算出采用哪种电流模式最适合。
研究人员还在探索新的重建技术。切尼正在主持研究一种很有发展前景的方法,称为分层剥离的技术。从概念上看,分层剥离就是一层层地依次求出电导分布,如同给洋葱削皮一般。在外表面测得的电流与电压直接用来解第一层的电导率。然后用这个解再来计算内一层的电流与电压值。于是得到下一层的电导分布,以此类推。“这是一个简单的想法,”切尼说,“美妙的是,它在许多问题中都很有用。”
RPI小组的研究人员并不是研究阻抗成像的唯一团队,不过切尼称赞艾萨克是最清楚了解这一领域的人。“他有能力做的最重要的事情之一就是能够提出最合理的问题。”她说,“人们思考反问题,通常从重建问题开始。考虑重建所需要的数据往往可以给出需要进行什么样的测量。可是大卫却从另一个角度来看这个问题,先构造一个系统,然后问怎样测量可以得到最多的信息。'
这个问题的解决也许最终可以拯救许多生命。
(声明:本文仅代表作者观点,不代表本站观点,仅做陈列之用)
[责编:]
郑重声明:本文版权归原作者所有,转载文章仅为传播更多信息之目的,如作者信息标记有误,请第一时间联系我们修改或删除,多谢。